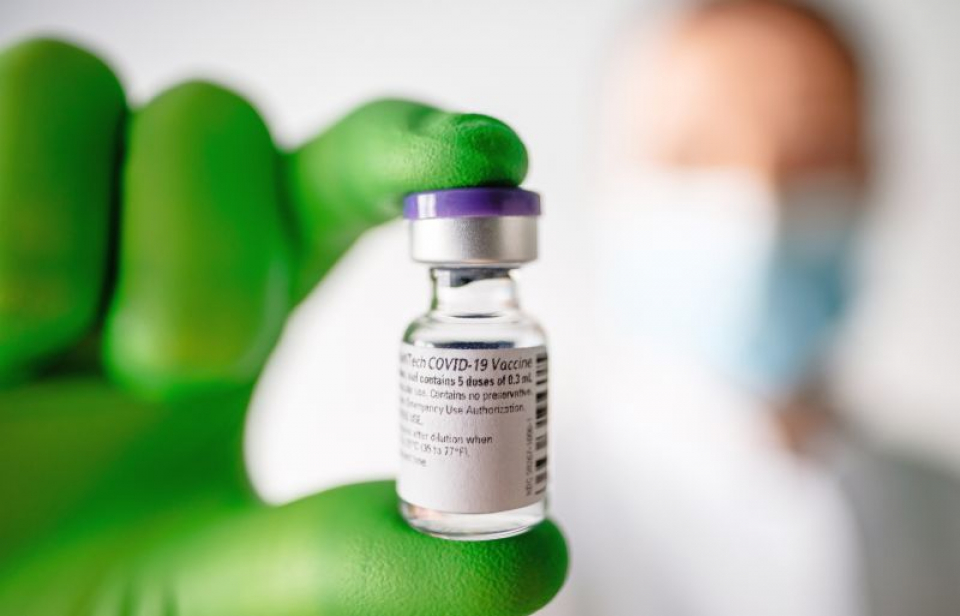
Comitetul pentru medicamente umane (CHMP) al EMA a recomandat, luni, o modificare a condițiilor de depozitare aprobate pentru Comirnaty, vaccinul COVID-19 dezvoltat de BioNTech și Pfizer, care va facilita manipularea vaccinului în centrele de vaccinare din Uniunea Europeană (UE).
Această modificare extinde perioada de depozitare aprobată a flaconului dezghețat nedeschis la 2-8° C (adică la temperatura dintr-un frigider normal după scoaterea din condiții de îngheț) de la cinci zile la o lună (31 de zile).
Modificarea a fost aprobată în urma evaluării datelor suplimentare ale studiului de stabilitate prezentate EMA de către titularul autorizației de introducere pe piață. Se așteaptă ca măsura să ducă la o flexibilitate sporită în depozitarea și manipularea vaccinului și să aibă un impact semnificativ asupra planificării și logisticii distribuirii acestuia în statele membre ale UE, se arată într-un comunicat (link direct).
Modificările descrise vor fi incluse în informațiile disponibile public despre Comirnaty și vor fi implementate de către titularul autorizației de introducere pe piață în etichetarea actualizată a produsului. Utilizatorilor li se reamintește să se refere întotdeauna la eticheta și prospectul produsului furnizat pentru informații corecte de depozitare.
„EMA este în dialog continuu cu deținătorii de autorizații de introducere pe piață pentru vaccinurile COVID-19, în timp ce încearcă să aducă îmbunătățiri de fabricație pentru a spori distribuția vaccinurilor în UE”, se mai arată în document.
Fiți la curent cu ultimele noutăți. Urmăriți DCMedical și pe Google News
Te-a ajutat acest articol?
Urmărește pagina de Facebook DCMedical și pagina de Instagram DCMedical Doza de Sănătate și accesează mai mult conținut util pentru sănătatea ta, prevenția și tratarea bolilor, măsuri de prim ajutor și sfaturi utile de la medici și pacienți.