Comitetul pentru medicamente umane (CHMP) al EMA (Agenției Europene a Medicamentului) a recomandat acordarea unei autorizații de introducere pe piață în Uniunea Europeană pentru Baqsimi (glucagon), primul tratament pentru hipoglicemie severă (niveluri scăzute de zahăr din sânge) care poate fi administrat fără o injecție pacienților cu diabet cu vârsta de patru ani și mai în vârstă.
Hipoglicemia severă este o complicație acută gravă a diabetului. Apare atunci când nivelul de zahăr din sânge scade la un nivel în care pacientul devine confuz sau inconștient și necesită asistență din partea altei persoane pentru administrarea unui medicament. Dacă este lăsată netratată, hipoglicemia severă poate duce la consecințe grave, inclusiv convulsii, comă, rezultate cardiovasculare adverse și chiar deces.
Glucagonul crește nivelul de zahăr din sânge în organism stimulând ficatul să elibereze glucoza stocată în fluxul sanguin. Are efectul invers al insulinei, care scade nivelul glicemiei.
În loc de glucagonul clasic injectabil, cu aceleași efecte
Glucagonul injectabil este în prezent singura opțiune de tratament pentru niveluri extrem de scăzute de zahăr în sânge, în afara unui spital sau a unui cadru medical de urgență. Utilizarea sa necesită adesea antrenament, deoarece trebuie pregătit în mai multe etape înainte de a putea fi administrat pacientului prin injecție subcutanată sau intramusculară.
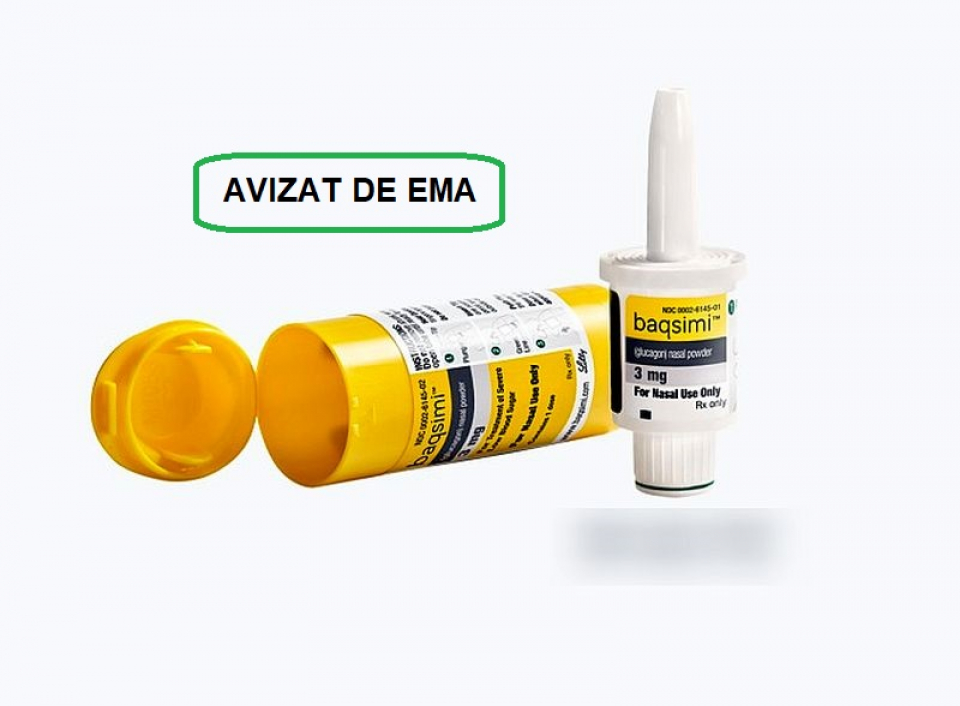
Baqsimi oferă o formulare farmaceutică nouă pentru glucagon. Medicamentul vine într-un distribuitor de o singură utilizare, care este gata de folosire și poate fi administrat prin nas, de către îngrijitorii persoanei cu hipoglicemie severă. Pacienții nu trebuie să inspire sau să respire profund după administrare, ceea ce permite administrarea de medicamente chiar și la pacienții inconștienți.
Eficacitatea și siguranța Baqsimi a fost evaluată în două studii la 83 și 70 de adulți cu diabet și hipoglicemie indusă de insulină. Baqsimi a crescut adecvat nivelul glicemiei în termen de 30 de minute de la administrare și s-a demonstrat a fi la fel de eficient și sigur ca glucagonul injectabil. Într-un studiu pediatric efectuat pe 48 de pacienți cu vârsta de patru ani cu diabet de tip 1, au fost observate rezultate similare, notează EMA.
Cele mai frecvente manifestări adverse au fost cefalee, greață, vărsături, iritații ale tractului respirator superior, ochi apoși, roșeață a ochilor și mâncărime. Efectele secundare ale Baqsimi sunt similare cu glucagonul injectabil, cu adăugarea de simptome nazale și legate de ochi din cauza modului de administrare a medicamentului.
Trimis spre aprobarea Comisiei Europene
CHMP a recomandat măsuri suplimentare de reducere a riscurilor, pentru a reduce și a preveni riscul potențial de utilizare necorespunzătoare a dispozitivului. Acestea includ un kit demonstrativ cu un dispozitiv de instruire, un prospect de administrare și un videoclip cu instrucțiuni. Trusa demonstrativă va fi distribuită în primul rând specialiștilor din domeniul sănătății care vor prescrie Baqsimi, dar va fi, de asemenea, pusă la dispoziția pacienților și îngrijitorilor acestora, la cerere.
Avizul adoptat de CHMP este un pas intermediar pe calea Baqsimi către pacienți. Avizul va fi trimis acum Comisiei Europene pentru adoptarea unei decizii privind o autorizație de introducere pe piață la nivelul întregii UE. Odată cu acordarea autorizației de introducere pe piață, deciziile privind prețul și rambursarea vor avea loc la nivelul fiecărui stat membru, ținând cont de rolul / utilizarea potențială a acestui medicament în contextul sistemului național de sănătate al țării respective.
Acest tratament a fost aprobat, în iulie 2019, și de FDA, în SUA.
Fiți la curent cu ultimele noutăți. Urmăriți DCMedical și pe Google News
Te-a ajutat acest articol?
Urmărește pagina de Facebook DCMedical și pagina de Instagram DCMedical Doza de Sănătate și accesează mai mult conținut util pentru sănătatea ta, prevenția și tratarea bolilor, măsuri de prim ajutor și sfaturi utile de la medici și pacienți.